Група на периодичната система
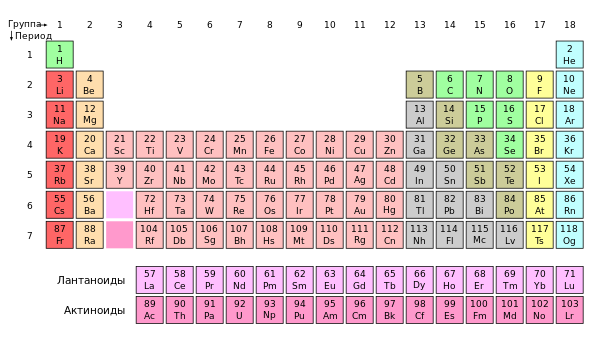
Групи в периодичната система на елементите се наричат вертикалните колони в периодичната система. Те са осемнадесет на брой. Група е последователността на атомите според нарастването на заряда на ядрото, като атомите притежават еднотипен електронен строеж. Номерът на групата се определя от броя на електроните във външния слой на атома (валентните електрони) и, като правило, съответства на най-високата валентност на атома.
Елементите в групата проявяват сходни свойства. С увеличаване на поредния номер на периодичната система химичният им характер закономерно се променя. С увеличаване поредния номер металният характер отслабва, а неметалният се увеличава.
С увеличаване заряда на ядрото на елементите от една група, поради увеличаването броя на електронните обвивки, се увеличават атомните радиуси, вследствие на което се намалява електроотрицателността, усилват се металните и се отслабват неметалните свойства на елементите, усилват се възстановителните и се отслабват окислителните свойства на образуваните от тях вещества.
Номерация на групите
[редактиране | редактиране на кода]От 1989 г. Международният съюз за чиста и приложна химия (IUPAC) като основен вариант на периодичната система утвърждава нова (дългопериодна) форма[1]. Във връзка с това IUPAC препоръчва непрекъсна номерация на групите с арабски цифри от 1 до 18. В съвременната световна литература късата форма е напълно изключена, вместо нея се използва само дългата форма.
В старата (къса) форма на периодичната система на елементите групите са осем, номерирани с римски цифри. Групите се делят на подгрупи – главни (или подгрупи A), започващи с елементите от първи и втори период, и странични (подгрупи В), съдържащи d-елементи. Подгрупите имат названия според елемента с най-малък заряд на ядрото (като правило, според елемента от втори период за главните подгрупи и елемента от четвърти период за страничните подгрупи). Елементите от една дадена подгрупа притежават сходни химични свойства.
Съвременната система на номерация съдържа следите групи (номерацията с римски цифри по старата европейска система е посочена в скоби):
- Група 1 (IA, алкални метали)
- Група 2 (IIA, алкалоземни метали)
- Група 3 (IIIB, подгрупа на скандия)
- Група 4 (IVB, подгрупа на титана)
- Група 5 (VB, подгрупа на ванадия)
- Група 6 (VIB, подгрупа на хрома)
- Група 7 (VIIB, подгрупа на мангана)
- Група 8 (VIIIВ, подгрупа на желязото)
- Група 9 (VIIIВ, подгрупа кобалта)
- Група 10 (VIIIВ, подгрупа на никела)
- Група 11 (IB, подгрупа на медта)
- Група 12 (IIB, подгрупа на цинка)
- Група 13 (IIIA, подгрупа на бора)
- Група 14 (IVA, подгрупа на въглерода)
- Група 15 (VA, подгрупа на азота)
- Група 16 (VIA, подгрупа на кислорода (халкогени)
- Група 17 (VIIA, халогени)
- Група 18 (VIIIA,[2] инертни газове)
Бележки
[редактиране | редактиране на кода]- ↑ Сайфуллин Р. С., Сайфуллин А. Р. Новая таблица Менделеева // Химия и жизнь.— 2003.— № 12.— С. 14 – 17.
- ↑ Подгрупата на хелия (инертни газове) понякога, особено в стари издания, се означава с цифрата 0.
Периодична система на елементите
| |||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| H | He | ||||||||||||||||||||||||||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||||||||||||
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||||||||||||
| Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | ||||||||||
| Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | ||||||||||
| |||||||||||||||||||||||||||||||||||||||||
