Липополизахарид

Липополизахаридите (ЛПЗ, също наричани „липогликани“) са големи органични молекули, съдържащи липид и полизахарид, съединени чрез ковалентна връзка. Те се намират върху външните стени на Грам-негативни бактерии, изпълняват функциите на ендотоксини и предизвикват силна имунна реакция у животните.
Функции
[редактиране | редактиране на кода]ЛПЗ изграждат основния компонент на външната мембрана на Грам-негативните бактерии и допринасят за запазването целостта на организма и предпазването му от вредни химични или механични въздействия. ЛПЗ също така увеличават отрицателния заряд (товар) на клетъчната мембрана и я стабилизират структурно. За Грам-негативните бактерии е от основна важност да съхранят непокътната липополизахаридната си обвивка, за да избегнат мутации или смърт. Липополизахаридите са важни за непатогенните аспекти на бактериалната екология, в които се включва способността им да се прилепват към предмети и да се предпазват от хищници от рода на амебата, както и да притежават определена чувствителност за присъствието на фаги. Правилната структура на бактериалната ендонуклеаза омптин зависи от наличието на ЛПЗ. Едновременно с това, не всеки вид ЛПЗ е подходящ за нормалното функциониране на омптин; гладки ЛПЗ пречат пространствено на разгъването на ендонуклеазата.
ЛПЗ се държат като „прототипни токсини“, защото се свързват с рецепторния комплекс CD14/TLR4/MD2, който отговаря за стимулиране на провъзпалителни цитокини в много клетъчни типове, но особено много реагират макрофагите. Също така се смята, че ЛПЗ са първопричинители на фебрилните симптоми у пациенти, заразени с Грам-негативни патогени. ЛПЗ се използват в рамките на имунологията; „ЛПЗ предизвикателство“ се нарича администрирането на потенциални токсини (в лицето на ЛПЗ) върху пациента за установяване на реактивността му към тези вещества.
Поради жизненоважното значение на ЛПЗ за оцеляването на грам-негативните организми, те са обект на проучване за формулиране на нови антибиотични терапии.
Някои изследователи подлагат на съмнение токсичността на всички ЛПЗ, особено що се отнася до цианобактериите.[1]
Структура
[редактиране | редактиране на кода]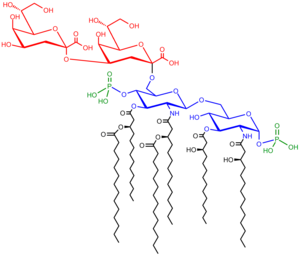
Съдържа три части:
О-антиген
[редактиране | редактиране на кода]Полимер, състоящ се от повтарящи се гликани и намиращ се в състава на ЛПЗ, се нарича O антиген, O полизахарид или О-странична верига на бактерията. О-антигенът се закачва към ядрения олигозахарид и образува най-външната част на ЛПЗ молекулата. Химическата структура на O-антигена варира според бактериалните щамове. Така например според типа само на O-антигена у Ешерихия коли, се наблюдават около 160 различни щамове.[2] Според присъствието или отсъствието на O-антигенните вериги се определя дали ЛПЗ е гладък или зърнест (неравен). Дълги вериги на О-антигени правят структурата на ЛПС гладка и обратно.[3] Бактерии с неравни ЛПЗ обикновено са по-уязвими за хидрофобни антибиотици, тъй като ЛПЗ, а оттам мембраната на бактерията, е по-хидрофобна.[4] O-антигените са изложени на разпознаването и атаката от защитните системи на гостоприемника, тъй като антителата на готоприемника контактуват с най-външната част на бактериите.
Ядрен олигозахарид
[редактиране | редактиране на кода]Ядреният домейн на ЛПЗ винаги притежава олигозахариден компонент, който директно се закрепва за липида А и обикновено съдържа захари от рода на хептозата и 3-деокси-D-манооктулосонна киселина (позната също под името Кето-деокси-октулосонат или КДО).[5] Сърцевината на ЛПЗ на много бактерии понякога съдържа и не-въглехидратни елементи като фосфати, аминокиселини и етаноламинови заместители.
Липид А
[редактиране | редактиране на кода]При нормални обстоятелства липид А е фосфорилиран глукосаминов дизахарид, точкуван с множество мастни киселини. Тези хидрофобни киселинни вериги закрепват ЛПЗ върху бактериалната мембрана, а останалата част на ЛПЗ се насочва към заобикалящата среда. Участъкът на липид А е отговарен за основната токсичност на грам-негативните бактерии. При разрушаването на стената на бактерията, липидните остатъци се отделят под формата на ендотоксини и причиняват основните болестни симптоми като треска, диария и дори циркулаторен колапс – шок и възможен фатален край.
Имунна реакция
[редактиране | редактиране на кода]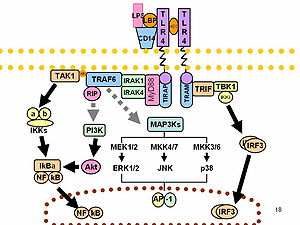
В последните няколко години ЛПЗ са обект на усилени проучвания поради ролята им в активиране на много транскрипционни фактори. ЛПЗ предизвикателства произвеждат много от инфламаторните медиатори отговорни за патологичните процеси на септичния шок. Човешкият организъм е много по-чувствителен към ЛПЗ, за разлика от други животни, като например мишките. Минималната доза от 1 µg/kg довежда до шоково състояние човека, докато мишките са в състояние да толерират хилядократно по висока доза.[6] Причината за това вероятно е разликата между двата вида в циркулиращите антитела.[7][8] Колектив, ръководен от Е. А. Саид (Said et al.), демонстрира, че ЛПЗ причинява зависимото от интерлевкин-10 (IL-10) потискане на експанзията на CD4 T лимфоцитите, посредством ап-регулация на нивата на PD-1 в моноцитите, което води до произвеждане на IL-10 от моноцитите след съединяване на PD-1 с PD-L.[9]
Източници
[редактиране | редактиране на кода]- ↑ Stewart I, Schluter PJ, Shaw GR. Cyanobacterial lipopolysaccharides and human health – a review // Environ Health 5. 2006. DOI:10.1186/1476-069X-5-7. с. 7.
- ↑ Christian Raetz and Chris Whitfield (2002) Lipopolysaccharide Endotoxins Annu. Rev. Biochem. 71:635 – 700
- ↑ Rittig MG et al. Smooth and rough lipopolysaccharide phenotypes of Brucella induce different intracellular trafficking and cytokine/chemokine release in human monocytes // Journal of Leukocyte Biology 5 (4). 2004. DOI:10.1189/jlb.0103015. с. 196 – 200.
- ↑ Tsujimoto H et al. Diffusion of macrolide antibiotics through the outer membrane of Moraxella catarrhalis // Journal of Infection and Chemotherapy 74 (4). 2003. DOI:10.1007/s101569900025. с. 1045 – 1055.
- ↑ Hershberger C and Binkley SB. Chemistry and Metabolism of 3-Deoxy-d-mannooctulosonic Acid. I. STEREOCHEMICAL DETERMINATION // Journal of Biological Chemistry 243 (7). 1968. с. 1578 – 1584.[неработеща препратка]
- ↑ Warren, HS и др. Resilience to bacterial infection: difference between species could be due to proteins in serum. // J Infect Dis 201 (2). 2010. DOI:10.1086/649557. с. 223–232.
- ↑ Reid RR, Prodeus AP, Khan W, Hsu T, Rosen FS, Carroll MC. Endotoxin shock in antibody-deficient mice: unraveling the role of natural antibody and complement in the clearance of lipopolysaccharide // J. Immunol. 159 (2). 1997. с. 970 – 5.
- ↑ Boes M, Prodeus AP, Schmidt T, Carroll MC, Chen J. A critical role of natural immunoglobulin M in immediate defense against systemic bacterial infection // J. Exp. Med. 188 (12). 1998. DOI:10.1084/jem.188.12.2381. с. 2381 – 6.
- ↑ Said EA et al. Programmed death-1-induced interleukin-10 production by monocytes impairs CD4+ T cell activation during HIV infection // Nature Medicine 16 (4). 2010. с. 452 – 9.
| Тази страница частично или изцяло представлява превод на страницата Lipopolysaccharide в Уикипедия на английски. Оригиналният текст, както и този превод, са защитени от Лиценза „Криейтив Комънс – Признание – Споделяне на споделеното“, а за съдържание, създадено преди юни 2009 година – от Лиценза за свободна документация на ГНУ. Прегледайте историята на редакциите на оригиналната страница, както и на преводната страница, за да видите списъка на съавторите.
ВАЖНО: Този шаблон се отнася единствено до авторските права върху съдържанието на статията. Добавянето му не отменя изискването да се посочват конкретни източници на твърденията, които да бъдат благонадеждни. |
