Натриев бикарбонат
| Натриев бикарбонат | |
| Свойства | |
|---|---|
| Формула | NaHCO₃ |
| Моларна маса | 83,982 u[1] |
| Плътност | 2,159 g/cm³ |
| Опасности | |
| H-фрази | H319[2] |
| P-фрази | P305+P351+P338[2] |
| NFPA 704 |
|
| Идентификатори | |
| CAS номер | 144-55-8 |
| PubChem | 516892 |
| ChemSpider | 8609 |
| DrugBank | DB01390 |
| KEGG | C12603 |
| MeSH | D017693 |
| ChEBI | 32139 |
| ChEMBL | CHEMBL1353 |
| RTECS | VZ0950000 |
| ATC | B05XA02 |
| SMILES | C(=O)(O)[O-].[Na+] |
| InChI | InChI=1S/CH2O3.Na/c2-1(3)4;/h(H2,2,3,4);/q;+1/p-1 |
| InChI ключ | UIIMBOGNXHQVGW-UHFFFAOYSA-M |
| UNII | 8MDF5V39QO |
| Данните са при стандартно състояние на материалите (25 °C, 100 kPa), освен ако не е указано друго. | |
| Натриев бикарбонат в Общомедия | |
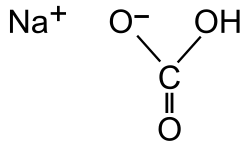
Натриевият бикарбонат (наименование по IUPAC – натриев хидрогенкарбонат; известен още като сода бикарбонат и сода за хляб) има химична формула NaHCO3. Той е ненаситена натриева сол на въглеродната киселина (H2CO3). В нормални условия е бяло твърдо вещество. Произвежда се чрез процеса на Солвей, при който смес от вода, амоняк и натриев хлорид (готварска сол) реагират с въглероден диоксид.
Водните разтвори на натриевия бикарбонат са алкални, защото той е сол на силна основа и слаба киселина. По тази причина той се използва за неутрализация на киселини (стомашни сокове), напр. при гастрит или язва.
Содата бикарбонат е честа съставка на бакпулвера. В състава му влизат още киселини (например лимонена киселина или кисели соли – хидрогенфосфати и др.), които при овлажняване реагират със содата, при което се отделя въглеродна киселина. Последната се разлага на вода и въглероден диоксид и обуславя процеса бухване, водещ до образуването на шупли в изпечените продукти.
При нагряване до 270 °C натриевият бикарбонат се дехидрира до натриев карбонат (Na2CO3, калцинирана сол) и въглероден диоксид (CO2). При по-нататъшно нагряване натриевият карбонат се разлага до динатриев оксид (Na2O) и въглероден диоксид[3].
Намира широко приложение в химическата (бои, пластмаси, битова химия, пожарогасители), хранителната (хлебни и сладкарски изделия, газирани напитки), леката (автомобилни гуми, изкуствени кожи, текстил) промишлености, фармацевтиката, цветната металургия.
Натриевият бикарбонат е регистриран като хранителна добавка E500.[4][5]
Източници
[редактиране | редактиране на кода]- ↑ SODIUM BICARBONATE // PubChem. Посетен на 4 октомври 2016 г. (на английски)
- ↑ а б www.mach-chemikalie.cz // Посетен на 25 август 2020 г. (на чешки)
- ↑ General Chemistry Online
- ↑ Информация за храните
- ↑ Codex Alimentarius




